Chmiel zwyczajny - Działanie i farmakologia
Chemizm:
Zawartość substancji czynnych w szyszkach chmielu ulega dużym wahaniom w zależności od odmiany, warunków wegetacji oraz sposobu zbioru, suszenia i przechowywania. Szyszki chmielowe zawierają olejek eteryczny (0,5-2%), w którego skład wchodzi około 26 związków terpenowych i sekswiterpenowych (humulen, mircen, kariofilen i inne) i żywice 10-22%, składające się z tzw. kwasów goryczowych (humulon, lupulon i ich pochodne), oraz garbniki (2-5%) i flawonoidy.
W lupulinie znajdują się te same związki co w szyszkach chmielowych, tylko w innych proporcjach. I tak np. olejku jest 1-6%, żywic do 80%, ponadto występują tłuszcze białka, polisacharydy. W czasie przechowywania poszczególne składniki ulegają rozkładowi i przemianom, co zmniejsza wartość lupuliny (Rumińska A. i inni, 1990).
Acylofloroglucynole (10%)
Alfa-kwasy: zawiera między innymi humulon, kolumulon, adlumulon (z dwoma łańcuchami dimetyloallilowymi)
Beta-kwasy: zawiera między innymi lupulon, kolupulon, adlupulon (z trzema łańcuchami dimetyloallilowymi)
Najważniejsze alfa, beta i gamma kwasy występujące w żywicy:
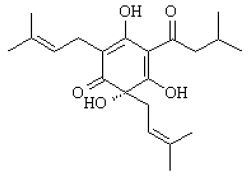
Humulon C21H30O5, Masa molowa 362.47 CAS# 469-02-03
m.p. 63, 70-71, 60-61, 64.5, 64-65, 72, 73
UVλmax(ε) 228(14125), 327(10715), 356 (8912) (EtOH); 236, 285, 323 (15,600 -?) (MeOH); 237,282,330 (EtOH); 228,324 (alkali/ EtOH); 235,281.5 (H+/ EtOH);[α]D -206 (c=0.38, MeOH).; -212.; -211.; -211(MeOH); +226(benzen); -91(pirydyna) ; +53 (piperydyna);pK 4.22(25oC), 4.26(40oC)
produkt naturalny, (-)-humulon
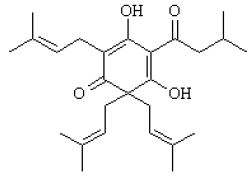
Lupulon C26H38O4, Masa molowa 414.58 CAS# 468-28-0
m.p. 90-91, 93, 93, 93, 93, 94,UVλmax(ε) 228,280,338 (EtOH); 231,283,340(15,500-?) (MeOH)pK 6.18(25oC), 6.3(40oC)
Olejek (0,3 - 1%): zawiera terpeny i seskwiterpeny, główne składniki to humulen, betakaryofilen, undekan-2-on, ponadto 2-metylo-3-butenol (szczególnie po przechowywaniu jako produkt rozkładu acylofloroglucynoli), mircen i farnezen
Najważniejsze związki wystepujące w olejku z Humulus lupulus:
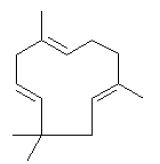
Humulen (a-kariofilen) C15H24, Masa mol. 204.35
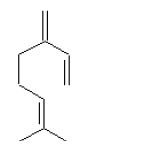
Mircen C10H16, Masa molowa 136.24
CAS # 123-35-3
Żywice (produkty oksydacyjnego rozpadu kwasów goryczowych)
Kwasy fenolowe: zawiera między innymi kwas ferulowy, kwas kawowy i ich pochodne
Garbniki: oligomeryczne proantocyjanidyny
Flawonoidy: pochodne kwercetyny i kemferolu oraz ksantohumol (z grupy chalkonów):
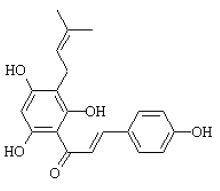
Ksantohumol C21H22O5, Masa molowa 354.41
CAS#'s 569-83-5, 6754-58-1m.p. 167-169, 157-157, 172, 171, 176, 147-148UVλmax(ε) 368; 368(38994) (MeOH); 372(EtOH/H+),440(EtOH/alk.)Główny flawonoid chmielu, 0.3 - 1% suchej masy.Żółto pomaranczowe kryształy. Jesli jest obecny w procesie warzenia piwa (tj. kiedy jest używana cała roślina), ulega prawie całkowitej przemianie do izoksantohumolu.Pierwsza wzmianka: Verzele i współpracownicy;Bull.Soc.Chim.Belg.; 66; 1957; 452,457;UV spectra: Bull.Soc.Chim.Belg.; 66; 1957; 452,460;2DNMR: Phytochem.;44; 8; 1997; 1575-1586;
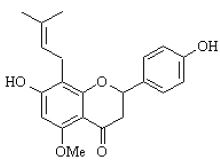
Izoksantohumol C21H22O5, Masa molowa 354.41 m.p. 198, 196, 178-180, 150-155UVλmax(ε) 287(26485) (MeOH); 387(MeOH);Nie jest obecny w znaczących ilościach w świeżym chmielu, tworzy się w procesie warzenia piwa (Eagon C. L., 1997).
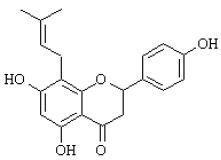
8-prenylonaryngenina C20H20O5, Masa mol. 340.38 m.p. 189, 193, 193-195, 194-196, 202-204, 183-184UVλmax(ε) 291 (MeOH); 295(18100) (MeOH; 215, 223, 225, 230, 240, 245, 294, 312. 314, 315, 316, 330, 332, 333, 335, 336, 338, 362, 385; 336(NaOH/ MeOH); 227(16218), 288(12023); 293(40738)[α]D -26 (c=1.0, MeOH, alpha-prenyl)
Tworzy się z desmetyloksantohumolu w procesie warzenia piwa. W badaniach wykazała silniejsze właściwości estrogenne od kumesterolu i genisteiny (Milligan S. R., 1999).
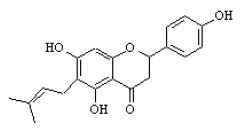
6-prenylonaryngenina C20H20O5, Masa mol. 340.38 m.p.UVλmax(ε)
8-geranylonaryngenina
6-geranylonaryngenina
Genisteina, biochanina A,
daidzeina,
formononetyna - Prawdopodobnie nie występują
Triterpeny m.in. hopanon (Gruenwald J. i inni, 2000).
Efekty działania:
Szyszki chmielowe są niezbędnym surowcem do wyrobu piwa. Nadają mu gorzki smak, aromat, trwałość i klarowność oraz zdolność pienienia się. Specyficzną właściwością chmielu jest to, że hamuje rozwój drobnoustrojów proteolitycznych, nie szkodząc komórkom drożdżowym.
W lecznictwie szyszki chmielowe mają małe zastosowanie, nieco większe ma lupulina. Działają uspokajająco na układ nerwowy, zwłaszcza w nadmiernej pobudliwości płciowej i w okresie przekwitania, nasennie i łagodnie moczopędnie. Piwo, dzięki lupulinie, ma podobne właściwości. Wyciąg z szyszek, ze względu na silne właściwości bakteriobójcze, stosuje się na wrzody i trudno gojące się rany (Rumińska A. i inni, 1990).
Badania:
W eksperymentach na zwierzętach 2-metylo-3-buten-2-ol, lotny związek, wydzielany przez rośliny, powodował po krótkim okresie pobudzenia długi i głęboki sen narkotyczny (Gruenwald J. i inni, 2000).
Gorzkie kwasy chmielowe mają działanie przeciwbakteryjne i przeciwgrzybicze. Stymulują wydzielanie soków żołądkowych. Sprawozdania z badań na zwierzętach donosiły o silnym efekcie spazmolitycznym na mięśnie gładkie jelita (Gruenwald J. i inni, 2000).
Za wiarygodne uważa się także działanie estrogenne (Gruenwald J. i inni, 2000).
Żeńskie kwiaty chmielu są używane jako środki konserwujące i nadające smak piwu. Jednakże, sugestia, że chmiel posiada silne działanie estrogenne ciągle powraca i że również piwo także może mieć działanie estrogenne. W przeprowadzonych badaniach czułe i specyficzne biooznaczenia in vitro zostały wykorzystane dla rozdzielenia estrogenów w zależności od działania przez selektywną ekstrakcję rozpuszczalnikiem lub rozdzielenie przy użyciu technik HPLC. Zidentyfikowano potencjalny fitoestrogen w chmielu, 8-prenylonaryngeninę, która ma aktywność większą niż inne estrogeny roślinne o ustalonej budowie. Działanie estrogenne tego związku zostało odzwierciedlone przez relatywne powinowactwo w wiązaniu do receptorów estrogennych macicy szczurów. Obecność 8-prenylonaryngeniny w chmielu może dostarczać wyjaśnienia dla przypadków zaburzeń menstruacji u kobiet, zbierających chmiel. Ten fitoestrogen można wykryć także w piwie, ale jego poziom jest niski (Milligan S.R. i inni, 1999).
Określenie zawartości 8-prenylonaryngeniny w piwie przy użyciu chromatografii i spektrometrii masowej:
Opracowano specjalną metodę dla określenia zawartości 8-prenylonaryngeniny w piwie. Jej zawartość w próbkach piwa wahała się pomiędzy 61,1 +/-6,6 a 82,2 +/-8,8% odpowiednio dla poziomów 37 i 92,5 µg/l, a granica wykrywalności wynosiła 5 µg/l. Chociaż większość próbek piwa nie zawiera 8-prenylonaryngeniny w wykrywalnych ilościach, najwyższe stężenie jakie określono miało wartość 19,8 µg/l. Stężenie 8-prenylonaryngeniny w różnych gatunkach piwa, a także prawdopodobnie jej brak zależą od wyboru odmiany chmielu, zawartości chmielu lub typu produktów chmielowych wykorzystywanych w browarnictwie. Wydajność przechodzenia 8-prenylonaryngeniny z chmielu do piwa waha się pomiędzy 10 a 20% (Tekel’ J. i inni, 1999).
Określenie aktywności estrogennej piwa:
Przebadano 5 różnych piw australijskich w celu określenia aktywności estrogennej przy wykorzystaniu systemu dwuplasmidowego drożdży, w którym osadzono ludzki receptor estrogenowy alfa, po zagęszczeniu przez ekstrakcję fazy stałej. Następnie koncentrat piwny frakcjonowano przy użyciu HPLC w odwróconych fazach, dalej frakcje zostały określone przez próby biologiczne i GC-MC. Frakcja o najsilniejszym działaniu nie zawierała znanych fitoestrogenów. Całkowita aktywność odpowiadała średniej aktywności 43 ng 17β-estradiolu na litr piwa. Wyciągnięto wniosek, że wpływ związków, zawartych w piwie, na receptor estrogenowy alfa jest bez znaczenia dla ryzyka dla zdrowia, wynikającego ze spożywania piwa (Promberger A. i inni, 2001).
Endokrynna aktywność 8-prenylonaryngeniny i inny flawonoidów chmielu:
Żeńskie kwiaty chmielu od dawna są używane jako środek konserwujący i nadający smak piwu, ale teraz zaczynają być włączane do preparatów ziołowych dla kobiet na „powiększenie piersi”. W przeprowadzonym badaniu rozpatrywano relatywną aktywność estrogenną, androgenną i progestogenną znanego fitoestrogenu, 8-prenylonaryngeniny i strukturalnie podobnych flawonoidów. 6-prenylonaryngenina, 6,8-diprenylonaryngenina i 8-geranylonaryngeniny wykazywały pewną aktywność estrogenną, która jednak była mniejsza niż 1% aktywności 8-prenylonaryngeniny. Natomiast sama 8-prenylonaryngenina silnie współzawodniczyła z 17β-estradiolem o wiązanie z oboma typami receptora estrogenowego (α i β). Żaden ze związków (ksantohumol, izoksantohumol, 8-prenylonaryngenina, 6-prenylonaryngenina, 3’-geranylochalkonaryngenina, 6-geranylonaryngenina, 8-geranylonaryngenina, 4’O-metylo-3’prenylochalkonaryngenina i 6,8-diprenylonaryngenina), ani też ekstrakty polifenolowe z chmielu nie wykazały aktywności progesterogennej i androgennej. Rezultaty wskazują, że endokrynne właściwości chmielu i jego produktów są spowodowane przez bardzo wysoką aktywność estrogenną 8-prenylnaryngeniny i dlatego należy wyrazić zaniepokojenie dotyczące niekontrolowanego stosowania chmielu w preparatach dla kobiet (Milligan S.R. i inni, 2000).
8-prenylonaryngenina zwiększa czynność kompleksu E-cadheriny/kateniny:
Przebadano efekty 8-prenylonaryngeniny na agregację, wzrost i inwazyjność komórek MCF-7/6. Odkryto, że 8-prenylonaryngenina stymuluje agregację zależną od E-cadheryny i wzrost zawieszonych komórek MCF 7/6. Te efekty mogą być zahamowane przez czyste (swoiste) antyestrogeny ICI 182, 780. 8-prenylonaryngenina nie miała wpływu na inwazyjność komórek MCF 7/6 w sercu pisklęcia w badaniach in vitro. We wszystkich tych aspektach 8-prenylonaryngenina naśladuje efekty 17β-estradiolu na komórki MCF-7/6 (Rong H i inni; 2001).
